目前治疗阿尔茨海默病相关痴呆的药物可以暂时改善症状,但不能改变潜在的疾病进程。可溶性和不可溶性淀粉样β (Aβ)的积累可能启动或增强阿尔茨海默病的病理过程。一些证据表明淀粉样蛋白的去除可以减缓疾病的进展一种抗淀粉样抗体(aducanumab)已获得美国食品和药物管理局(FDA)的加速批准。
Lecanemab是一种人源化单克隆抗体,与可溶性淀粉样- β (a β)原纤维具有高亲和力。已被证明对神经元的毒性比单体或不可溶性原纤维更大,目前正在对早期阿尔茨海默病患者进行测试。
2022年11月29日,在 New England Journal of Medicine 杂志在线发表题为“Lecanemab in Early Alzheimer’s Disease”的研究论文。该研究进行了一项3期试验(Clarity AD),以确定lecanemab在早期阿尔茨海默病参与者中的安全性和有效性。

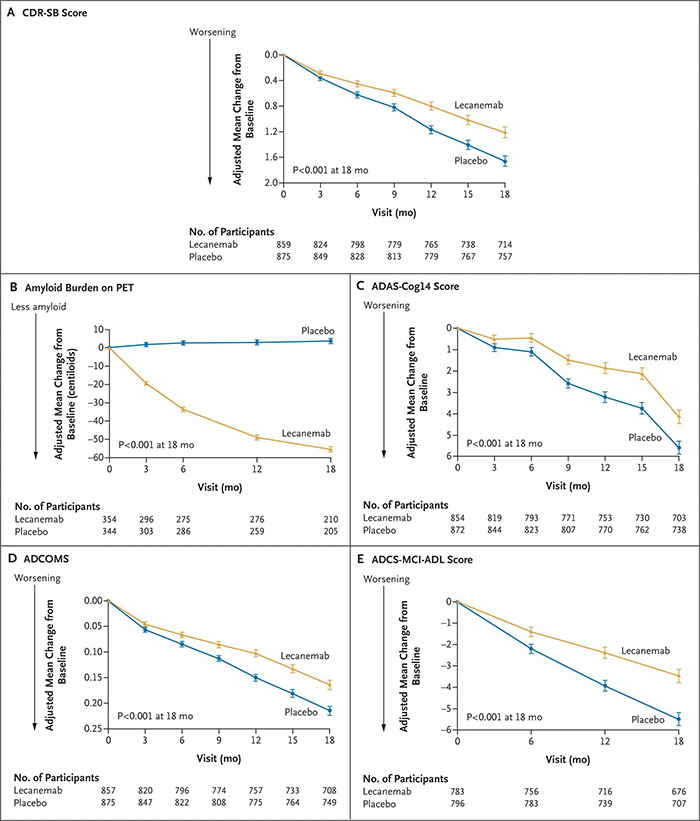
Lecanemab是一种人源化IgG1单克隆抗体,与a β可溶性原纤维具有高亲和力,目前正在对早期阿尔茨海默病患者进行测试。一项涉及854名早期阿尔茨海默病患者的2b期剂量发现试验,在12个月综合评分变化(主要终点)的贝氏分析中,未显示lecanemab与安慰剂之间存在显著差异。然而,18个月时的分析显示,使用lecanemab对淀粉样蛋白的清除依赖于剂量和时间,并且该药物在某些方面比安慰剂的临床衰退更小。在该试验中,每2周静脉给予每公斤体重10 mg的lecanemab为适当剂量,伴有水肿或积液(ARIA- e)的淀粉样相关影像学异常(ARIA)发生率为9.9%(<3%有症状)。该研究进行了一项为期18个月、多中心、双盲、三期试验,试验对象为50至90岁的早期阿尔茨海默氏症患者(因阿尔茨海默氏症导致的轻度认知障碍或轻度痴呆),正电子发射断层扫描(positron-emission tomography, PET)或脑脊液检测显示淀粉样蛋白。受试者按1:1的比例被随机分配静脉注射lecanemab(每千克体重10毫克,每2周一次)或安慰剂。该研究的主要终点是18个月时临床痴呆方框评分(CDR-SB;范围,0到18,分数越高表示损伤越大)。关键的次要终点是PET上淀粉样蛋白负担的变化,阿尔茨海默病评估量表14项认知亚量表的得分(ADAS-cog14;范围,0到90;得分越高表示损伤越大),阿尔茨海默病综合评分(ADCOMS;范围,0到1.97;轻度认知障碍的阿尔茨海默病合作学习-日常生活活动量表(ADCS-MCI-ADL;范围,0到53;分数越低,说明损伤越大)。该研究最终将1795名参与者纳入研究,其中898人接受lecanemab, 897人接受安慰剂。两组患者基线时平均CDR-SB评分约为3.2。18个月时,与基线相比,lecanemab组调整后的最小二乘平均变化为1.21,安慰剂组为1.66(差异,−0.45;95%置信区间[CI],−0.67 ~−0.23;P < 0.001)。在一项涉及698名参与者的亚研究中,与安慰剂相比,lecanemab更能减少大脑淀粉样蛋白负担(差异,−59.1, loids;95% CI,−62.6 ~−55.6)。主要和关键的次要终点(图源自 New England Journal of Medicine )两组患者从基线转向lecanemab的其他平均差异如下:对于ADAS-cog14评分,−1.44 (95% CI,−2.27至−0.61;P < 0.001);对于ADCOMS,−0.050 (95% CI,−0.074 ~−0.027;P < 0.001);adc - mci - adl评分为2.0 (95% CI为1.2 ~ 2.8;P < 0.001)。Lecanemab导致26.4%的参与者出现灌注相关反应,12.6%的参与者出现淀粉样蛋白相关影像学异常和水肿或积液。综上所述,该研究表明18个月时,Lecanemab降低了早期阿尔茨海默病的淀粉样蛋白标记物,与安慰剂相比,认知和功能指标的下降程度略有降低,但与不良事件有关。后续需要更长的试验来确定lecanemab在早期阿尔茨海默病中的有效性和安全性。DOI: 10.1056/NEJMoa2212948